“平时走路稳不稳?会不会突然摔倒?”“眼睛看得清楚吗?脑子反应快不快?”“好,现在看我手的示意,慢慢转动脑袋……”
7月盛夏,清晨窗外的阳光早已明晃晃地刺眼。复旦大学附属华山医院的住院部内,神经内科副主任郁金泰教授带着一群学生正在查房。

郁金泰教授(右一)和团队在复旦大学附属华山医院开学术研讨会
随着人口老龄化加剧,与年龄相关的神经退行性疾病负担持续上升。这位80后医学专家,17年来每天都在和阿尔茨海默病、帕金森病等“过招”。今年,继发现帕金森病全新治疗靶点后,阿尔茨海默病早筛早诊检测试剂也将于年底上线各大医院和体检中心,有助于提前预测发病风险。
这些突破性研究成果的背后,有一个“超级引擎”:复旦大学与阿里云等联合打造的CFFF智算平台。
“通过人工智能赋能,加速阿尔茨海默病预防诊治研究的进程,最终实现该病可防、可控、可治。”郁金泰满怀期待。在科技创新与医学进步的交融中,人类延长健康寿命的美好愿景正一步步变为现实。
提前15年预测阿尔茨海默病发病风险
“我感觉我的叶子都掉光了,那些树枝、狂风和暴雨。我已经搞不明白发生的一切。”2021年奥斯卡金像奖最佳男主角获奖影片《困在时间里的父亲》,主人公是一位阿尔茨海默病患者,随着病情的加重,他分不清过去和现在、幻想和现实……
生活中,千万患者正经历着同样的迷失——中国有近1700万痴呆症患者,阿尔茨海默病占比超60%。
这种起病隐匿、至今在临床治疗中无全解的神经退行性疾病,早发现早干预成为对抗它的关键。
今年2月,央视新闻一则关于复旦大学科研团队的报道点燃了希望之火:通过AI算法分析血浆蛋白质,未来或可实现仅需几滴血就能预测包括阿尔茨海默病在内的上百种疾病风险。
“阿尔茨海默病的发病率随着年龄呈指数级增长,70岁以上发病率可达15%,过了85岁可能达到20%-30%,95岁以后这个数字增长到45%。”郁金泰告诉橙柿互动记者。
通常阿尔茨海默病的确诊,依赖于临床问诊、神经评估以及一系列检查排除其他原因,但临床判断的准确率只有70%-80%。“想更准确的话,早期检测可以做PET(正电子发射计算机断层扫描)、腰穿查脑积液,但前者价格高昂且有辐射风险,后者有创性,不被部分患者或家属接受。”
有没有更优解?
郁金泰团队在外周血(除骨髓之外的血液)中发现了革命性的线索:某些关键蛋白质指标,在发病前15年就会有异常波动。这项发布于《自然·衰老》(NautureAging)的研究成果显示,通过血浆及脑脊液蛋白质组学研究发现阿尔茨海默病新的诊断生物标志物,联合诊断精度高达98.7%。
“这种检测兼具便捷性与经济性,未来或许可以大规模普及,尤其是在社区层面。”郁金泰认为。
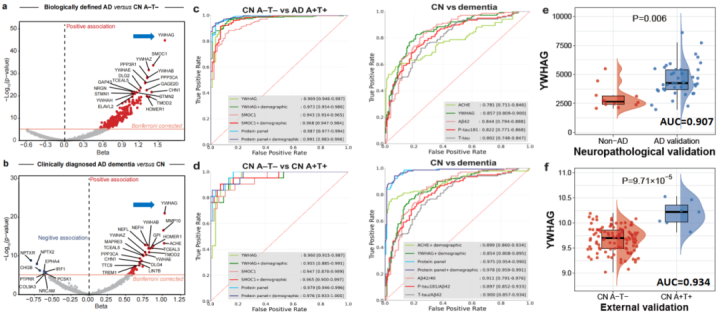
脑脊液蛋白对阿尔茨海默病诊断的准确度及外部队列验证和尸检病理验证结
以此为起点,团队纳入了5万人的约3000种测序蛋白,绘制了更宏大的蛋白质组图谱,试图通过血液检测实现数百种疾病的早期预警。
对我们普通人来说,这项研究成果的现实意义在于,不久的将来,一次普通的血检或许就能打开预防疾病的先知之门。而今年底,阿尔茨海默病早筛早诊检测试剂就会先行上线各大医院和体检中心。
数年完成的计算分析缩短至数周甚至数天
40公里外的复旦大学张江校区,类脑智能科学与技术研究院研究员程炜正在电脑前和学生们探讨优化模型。
郁金泰团队所取得的突破性研究成果,是人工智能赋予科研的全新视野,也是医工交叉碰撞出的火花。
应用数学出身的程炜,与郁金泰相识于5年前。双方团队兴趣相似、优势互补,一个医工交叉的课题组应运而生。

复旦大学附属华山医院郁金泰教授团队与复旦大学类脑智能科学与技术研究院冯建峰教授团队合影。前排左二为郁金泰,右二为程炜。
过去人们没有开展蛋白质组研究,主要受限于蛋白质检测技术和分析手段,海量数据难以处理,而如今AI让这一困境迎刃而解。“当时,我们利用血液中的蛋白质组学数据,测了约3000个不同的蛋白,通过算法分析识别出10个与阿尔茨海默病发病高度关联的蛋白质标志物。”程炜解释,如果用传统方法可能会找到数百个关联蛋白,无法精准判断哪些才是核心。
支撑这一突破的“超级大脑”是CFFF智算平台,阿里云提供的AI算力将原本需要数年的计算任务压缩到数周甚至是数天。这种算力跃迁让程炜感触颇深:“2011-2012年那会儿,我们团队自己买了几台机器,处理100人的影像数据就已很难,一台小服务器跑了好几天。”依托CFFF平台运行后,他有信心建立更大的数据库来推动研究。
目前,团队的研究数据主要来自两大渠道:公开数据(国内外开放数据库),以及专有数据。后者包括类脑研究院数万人脑影像库、华山医院临床数据,以及HEAD队列数据(在全国范围建立的社区脑健康衰老队列)。
“以前的研究过程像是在大海捞针,寻找特定的科研线索犹如钓鱼,可能需要很长时间才能找到想要的结果。而现在,AI技术就像一网打尽,能在短时间内高效筛选出大量相关数据,精准定位到目标,大大节约科研人员的时间和精力,也增强了科研人员解决问题的能力。”郁金泰表示。
重塑科研范式
“这是中国也是全球第一次让高校拥有了和科技巨头一样的研究计算平台,让研究真正进入计算驱动的时代。”两年前的6月CFFF上线当天,中国工程院院士、阿里云创始人王坚如是说。两年来,它已覆盖生命科学、材料科学等多个领域,推动百余项科研成果落地。
CFFF包含两个计算机集群:面向多学科融合创新的“切问1号”,以及面向计算科学高精尖研究的专用高性能计算机集群“近思1号”。借助阿里云全球领先的大规模异构算力融合调度技术、分级存储技术、AI与大数据一体化技术,两个集群连成了一台真正意义上的“超级计算机”。
其中,阿里云乌兰察布数据中心以公共云模式,为全国科研机构的多个项目提供超千卡并行智能计算,支持千亿参数的大模型训练。千卡并行的有效算力达到行业领先的92%,可拓展性达到万卡,万卡并行有效算力也可达90%。
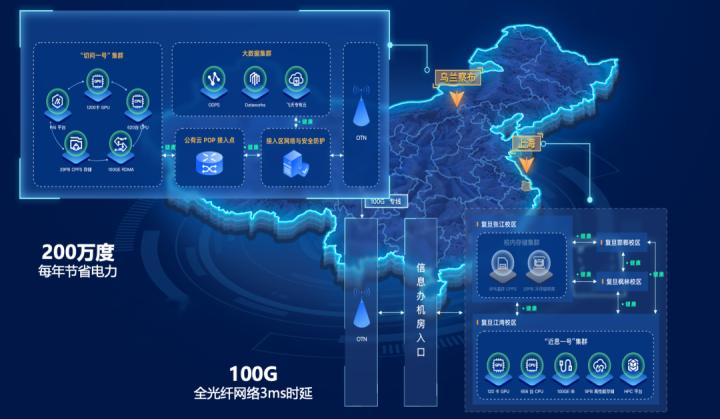
据橙柿互动了解,研究团队在CFFF平台上开设账号,团队负责人可设置不同的子账号分配给各组研究员使用。相比CFFF建成前各团队需自行购买服务器排队使用,CFFF提供了更充足的算力,可以实现多任务同时计算。一个账号对应一个域,数据都在一个账号域内,计算环境也更安全。
在程炜看来,随着AI时代对算力需求的增长,以及对数据安全和隐私保护的重视,很多高校都在建立或强化自己的计算平台。“尤其是在涉及敏感临床数据的研究中,自己拥有计算平台必不可少。”
对于研究人员而言,CFFF也正在引发一场科研范式的变革。
郁金泰说,传统研究采用“假设驱动”模式,研究人员需根据预设的理论推测可能的指标、靶点或药物;而AI介入后,研究范式转变为“数据+算法”驱动,借助深度学习算法和强大的算力支持,在海量数据中快速精准地发现关键指标和潜在治疗方案。
AI驱动精准医学的下一站
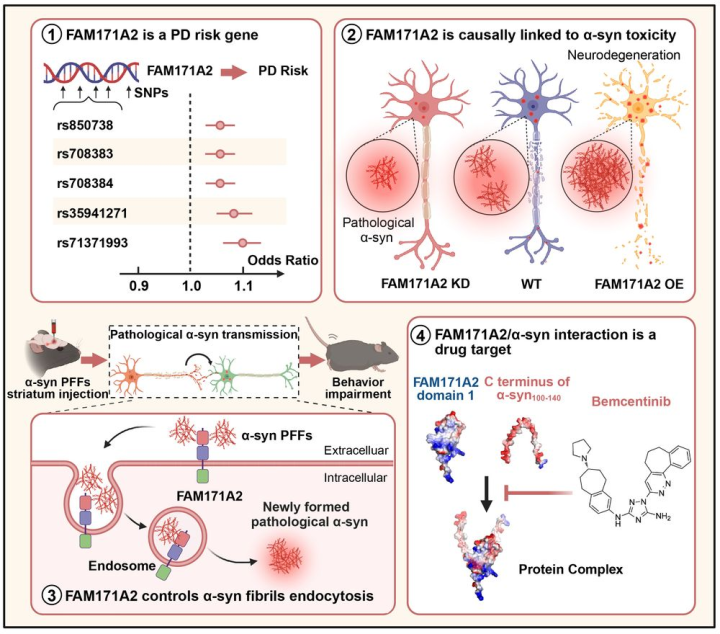
在全力攻克阿尔茨海默病的同时,郁金泰和程炜团队的目光投向了另一个困扰人类的顽疾——帕金森病。作为全球第二大神经退行性疾病,它同样缺少早期预警与精准治疗的“利器”。
这次,研究团队成功发现了帕金森病全新治疗靶点,并利用AI筛选出候选药物,登上《细胞》和《自然》等国际顶刊。这项原本需要数十年的研究,在AI加持下仅用5年就取得突破性进展。
眼下,程炜团队还在CFFF平台构建了一个基于血液多组学的多疾病预测模型。该模型仅需通过血液样本,就能对200多种疾病进行10年内的风险预警,准确率超80%。“我们搭建了一个交互式平台,用户可以上传体检报告或血液检查结果,系统将根据模型提供疾病风险预警服务。它基于真实生物学数据,而非大语言模型的预测。”
郁金泰则透露,将进一步利用人工智能新模型和新算法,整合多组学数据,促进精准医学发展。人类健康与疾病的代谢组图谱和多组学图谱等,都在紧锣密鼓地绘制中。
与此同时,阿里云AI基础设施也已支撑CFFF平台全面升级,提供文理医工各学科47个特色学科模型和4万余个科学数据集开放使用,支持发表了多篇CNS级别的高水平论文。
“AI不是取代医生,而是成为有效助手,提升医疗科研工作的效率和精准度。”程炜表示。不只为征服星辰大海,更为守护人间烟火,这或许就是AI最温暖的价值所在。